Остеоинтеграция основана на высоком сродстве между человеческой костью и титаном, и ее применение навсегда изменило профессию стоматолога, предложив безопасный, предсказуемый и воспроизводимый метод восстановления безнадежных зубов. Первоначально немногие врачи практиковали имплантацию в стоматологии и использовали данный метод в основном в качестве варианта лечения полностью беззубой зубной дуги на нижней челюсти при помощи имплантатов, размещенных внутри лунок от удаленных зубов. Это ограничение по использованию было обусловлено значительно более низкими показателями успеха проводимых манипуляций на верхней челюсти, в сравнении с имплантатами установленными во фронтальном отделе нижнечелюстной кости, где плотность костной ткани самая высокая в полости рта и недостаточный объем костной ткани встречается редко.
Значительный прогресс в макро- и микро-строении произошел в 1990-х годах, главным образом благодаря усовершенствованию технологий обработки поверхности имплантатов, что значительно увеличило площадь поверхности имплантатов и тем самым оптимизировало процесс остеоинтеграции в зонах с низкой плотностью кости, таким образом показатели успешно проведенной имплантациии на верхней челюсти, наконец, сравнялись с показателями, достигнутыми при проведении имплантации на нижней челюсти. Совмещение наличия зубных имплантатов с присутствием естественных зубов в зубном ряду при лечении пациентов с частичной адентией или замена одного зуба на имплантат стали жизнеспособным вариантом лечения только тогда, когда была достигнута предсказуемость процесса остеоинтеграции независимо от плотности кости.
Достижения в области дизайна имплантатов упростили протоколы лечения при установке реставраций с опорой на имплантат, что позволило заниматься имплантологией многим врачам-стоматологам, а не ограниченному числу докторов. Однако объем кости по-прежнему диктовал выбор метода протезирования пациента, и имплантаты устанавливались без особого внимания к идеальному положению имплантатов и их углам наклона. Стоматологи-ортопеды и зубные техники изо всех сил пытались найти способы восстановления некоторых клинических случаев при наличичии малого объема костной ткани,
что привело к разработке индивидуальных реставрационных абатментов и других компонентов имплантата. Следовательно, много имплантатов было установлено и остеоинтеграция их прошла успешно, но они так и не были покрыты коронками. Только после того, как была предложена концепция восстановительной имплантологии, хирурги начали использовать хирургические шаблоны в качестве ориентира для имплантологии. Поскольку установка имплантатов, основанная исключительно на доступном объеме костной ткани не считалась более приемлемым критерием, хирурги-стоматологи столкнулись с новой задачей: преодолеть недостаток объема альвеолярной кости в наиболее идеально подходящей для размещения протезной конструкции зоне, где и должны быть установлены имплантаты.
Первые концепции
Первые концепции увеличения костной ткани в имплантологии были заимствованы из ортопедии и челюстно-лицевой хирургии, где увеличение объема костной ткани использовалось для лечения пациентов с травмами и резекцией опухолей. Аутогенная трансплантация кости из донорских зон вне полости рта (например, гребня подвздошной кости, ребер, голени) была наиболее воспроизводимым методом увеличения альвеолярного отростка. Однако предсказуемость редко достигала 50%, процедура вызывала значительную степень потери трудоспособности, а сама стоимость процедуры для пациента была высокой, поскольку она включала госпитализацию и необходимость в подключении хирурга-ортопеда общего для сбора материала для трансплантации. С предлагаемым использованием внутриротовых источников аутогенной костной ткани (например, симфиза, ветви нижней челюсти, области бугра верхней челюсти, торуса нижней челюсти) методика лечения была упрощена, а степень потери трудоспособности пациентов снижена.
Использование коммерчески доступных материалов для замещения костной ткани для увеличения объема костной ткани началось с проведения процедур пневматизации верхнечелюстной пазухи и увеличения объема костной ткани в области придаточных пазух. С развитием методов увеличения объема костной ткани в области придаточных пазух и улучшением качества используемых материалов предполагаемая выживаемость имплантатов, установленных в областях, увеличенных по объему кости придаточных пазух, составляет 90% по прошествии трех лет со времени нагрузки данной зоны реставрационными конструкциями. Материалы для замены и восполнения костной ткани альвеолярного отростка и улучшения контуров зоны будущего размещения имплантатов были разработаны на основе концепции направленной регенерации тканей (GTR) для лечения дефектов тканей пародонта, где удаление нежелательных клеток (например, эпителия, соединительной ткани) из раны с помощью барьерных мембран позволило обеспечить миграцию желательных групп клеток (например, периодонтальная связка, кость) для улучшения результатов восстановительной терапии пародонта. Управляемая регенерация кости (GBR) проста по сравнению с GTR, поскольку в данном случае культивируется один тип ткани. Трансплантаты для замещения кости, полученные от других людей (аллотрансплантат), животных (ксенотрансплантат) или синтетических материалов, используются в качестве каркасов (остеокондукция) во время набора клеток из соседних костных перегородок, миграции, пролиферации и последующего созревания костной ткани. Биологические материалы (например, белки, факторы роста) в сочетании с костными каркасами обеспечивают дополнительный стимулирующий эффект во время процесса заживления раны (остеоиндукции). Успешная консолидация материала трансплантата зависит от постепенного соединения новообразованной кости с последующим функциональным ремоделированием и постепенной заменой ткани материала трансплантата жизненно важной костной тканью. Этот процесс требует наличия стабильного костного каркаса, адекватного формирования нового кровоснабжения и миграции клеток с остеогенным потенциалом.
Успешное созревание и консолидация участков трансплантации зависит в первую очередь от правильного формирования функционального комплекса трансплантат-жизненно важная костная ткань.
Материалы костных блоков и мембраны
При выборе материала для трансплантации для направленной костной регенерации тканей (GBR) предпочтение отдавалось плотным минерализованным материалам (например, бычьей кости), чтобы максимально сохранить пространство в процессе заживления ран и повысить плотность кости в расширенных областях. Бычья кость – это продукт природного происхождения, который сохраняет кристаллическую структуру, пористость и содержание карбонатов, аналогичные минералам костей человека, что способствует остеокондукции. На выбор плотных материалов повлияли исторически более низкие показатели успеха остеоинтеграции в костях с меньшей плотностью. Плотные материалы для трансплантации подвергаются чрезвычайно медленному процессу превращения материала для трансплантации, который может занять годы или десятилетия, а некоторые могут никогда полностью не превратиться в костную ткань.
Превосходная плотность костной ткани, достигаемая с помощью этого типа плотного материала для трансплантации, в значительной степени обусловлена остаточными частицами материала для трансплантации, а не превосходным качеством кости. Остаточные частицы материала трансплантата обеспечивают дополнительное сопротивление при подготовке к остеотомии имплантата и механическую стабилизацию во время установки имплантата, создавая у врача впечатление идеального качества кости. Качество кости определяется высоким процентом жизненно важной кости в расширенных хирургически областях, а не плотностью кости, возникающей из-за сопротивления во время подготовки к остеотомии имплантата и механической стабилизации во время установки имплантата. Только жизненно важные ткани функциональны и могут подвергаться ремоделированию кости. Следовательно, участки, дополненные плотными минерализованными материалами для трансплантата, обеспечивают более низкое качество кости по сравнению с участками, дополненными материалами для трансплантата, которые обладают способностью к преобразованию. Для этих участков были предложены и рекомендованы как более широкие (>4 мм), так и более длинные (>11 мм) имплантаты, чтобы компенсировать низкое качество кости в местах трансплантации тканей.
Барьерные мембраны играли второстепенную роль при использовании плотных материалов для трансплантации, действуя как перевязочный материал, удерживающий трансплантат, а не защищающий его от нежелательных клеток. Барьерная функция стала актуальной с развитием и переходом на материалы для трансплантации с более низкой плотностью, такие как минерализованный аллотрансплантат на основе губчатого вещества и деминерализованный аллотрансплантат. Благодаря гораздо более быстрому обращению этих материалов в ткань, как рассасывающиеся (коллаген), так и не рассасывающиеся (e-PTFE, d-PTFE) мембраны имеют решающее значение для клинического успеха, предотвращая инкапсуляцию материала трансплантата мягкими тканями лоскута и способствуя сохранению пространства. Технические корректировки были необходимы для достижения максимальных результатов операции. Стабилизация барьерной мембраны оказалась ключевым элементом клинического успеха, обеспечивая стабильность раны во время ее заживления. Предсказуемость лечения, превосходное качество кости, долгосрочная стабильность, низкая заболеваемость и воспроизводимость сделали процесс направленной костной регенерации (GBR) с использованием барьерной мембраны и материалов для замещения костной ткани низкой плотности стало новым методом “золотого стандарта” для коррекции дефектов альвеолярного отростка легкой и умеренной степени при восстановлении целостности зубных рядов при помощи имплантатов.
Сшивание коллагеновых волокон
Пролонгированная функция барьера необходима при использовании костных трансплантатов с высокой скоростью текучести. Теоретически, этого можно достичь более эффективно с помощью не рассасывающихся барьерных материалов поскольку эти материалы должны исключать клетки мягких тканей из увеличенной в объеме операционной зоны до тех пор, пока они не стабилизируются в данной области. Однако такие мембраны обладают меньшей биосовместимостью по сравнению с рассасывающимися мембранами (коллаген) и были связаны с более высокой частотой послеоперационных осложнений, вызванных расслоением раны, преждевременным обнажением барьерной мембраны и инфекцией, вторичной по отношению к раннему воздействию мембраны. Чтобы замедлить процесс рассасывания коллагеновых мембран и продлить барьерную функцию, используется сшивание коллагена. Наиболее часто используемым методом сшивания коллагена является использование глутарового альдегида. Ограничением этого метода является потенциальная цитотоксичность этих химических веществ для новообразованной ткани во время абсорбции мембраной. Альтернативный метод сшивания на основе рибозы значительно улучшает биоразлагаемость коллагеновой мембраны, не влияя на биосовместимость. Рассасывающиеся мембраны на тканевой основе (например, перикард, дерма) также обеспечивают длительную барьерную функцию без выделения нежелательных химических веществ в хирургическую рану. Без этих достижений в области рассасывающихся мембран внедрение материалов для костных трансплантатов последнего поколения было бы невозможно.
Полностью рассасывающиеся костные каркасы
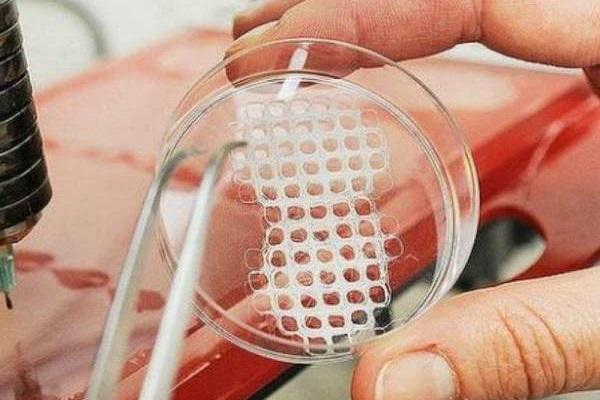
Полностью рассасывающиеся костные каркасы на основе коллагена обладают уникальными преимуществами по сравнению с традиционными методами замещения костной ткани. Поскольку конструкция состоит в основном из сшитого коллагена, время абсорбции можно регулировать во время изготовления путем изменения интенсивности сшивания. Эти материалы обеспечивают адекватные механические свойства для поддержания объема пространства, все еще подвергаясь активному процессу абсорбции / встраивания, который занимает от 4 до 6 месяцев в полости рта, что приводит к новообразованию кости без наличия остаточных свойств материала трансплантата. Сообщалось о многообещающих результатах в лечении лунки от удаления зуба, дефектов альвеолярного гребня легкой и умеренной степени тяжести после удаления, устранении зазора между непосредственно установленными имплантатами и стенками лунки, увеличении верхнечелюстной пазухи и коррекции дефектов прободения костной стенки со стороны щеки для достижения оптимальных эстетических результатов имплантации.
Другие примеры клинического применения данного метода, такие как лечение серьезных горизонтальных дефектов альвеолярного гребя и вертикальное увеличение объема альвеолярной кости, могут потребовать дальнейшего совершенствования хирургических методов лечения пациентов, в комбинации с совершенствованием биологических материалов для оптимизации процесса регенерации кости, и эти полностью рассасывающиеся материалы для замещения костной ткани в сочетании с долгосрочными рассасывающимися коллагеновыми мембранами могут в конечном итоге заменить традиционные методы увеличения объема альвеолярного гребня. Превосходное качество кости, достигаемое с помощью полностью рассасывающихся каркасов в методике направленной регенерации костной ткани (GBR), должно создать более стабильную костную ткань в зоне, окружающей имплантат, более устойчивую к периимплантным заболеваниям и потере объема кости, а также позволить использовать как более узкие (≤4 мм), так и более короткие (<10 мм) имплантаты в местах приживления имплантатов в подготовленных лунках, что сводит к минимуму риск для пациентов и облегчает повторное лечение в будущем, при необходимости такового.
Заключение
Ортопедическая-имплантологическая стоматология не оказала бы влияния на стоматологическое лечение множества пациентов за последние три десятилетия без разработки хирургических методов и материалов для увеличения объема альвеолярного отростка. Недавние достижения в этой области, включая разработку полностью рассасывающихся каркасов и долговечных рассасывающихся баръерных мембран, должны еще больше улучшить результаты лечения за счет обеспечения превосходного качества тканей, что позволит клиницистам использовать более короткие и узкие имплантаты в областях, увеличенного объема костной ткани.
Автор: Rodrigo Neiva, DDS, MS

